موتورهای ملکولی بیولوژیک، انرژی آزاد متابولیکی را به حرکت جهت دار شده تبدیل می کنند. فیزیکی که این تبدیل را کنترل می کند از اصول های موتورهای ماکروسکوپی ساخته دست بشر متفاوت است. یک میانکنش شیمیایی که انرژی را برای هر چرخه فراهم می کند موجب به جابه جایی اتم های شرکت کننده در مقیاس یک دهم نانومتر می شود. این درحالی است که یک مرحله از جابه جایی درون یک موتور پروتئینی معمولا تا چندین نانومتر گسترش پیدا می کند. هم چنین میانکنش نمی تواند دو قسمت از یک پروتئین رو به فاصله ی چندین نانومتر هل بدهد چون حرکت در این مقیاس هیچ اینرسی ندارد.
بنابراین از منظر القای مداوم انرژی شیمیایی، یک حرکت جهت دار یک زیر واحد پروتئینی تا زمانی ادامه پیدا می کند که نیرو به آن القا شود. از طرفی تمامی نیروهایی که در ارتباط با عمل شیمیایی هستند نیروهای کوتاه مدت هستند که تقریبا در طول فاصله ای کم تر از یک نانومتر ناپدید می شوند. در غیاب اینرسی و نیروهای طولانی مدت که به طور مستقیم از عمل شیمیایی به وجود می آیند موتورهای ماکروسکوپی ساخته دست بشر هرگز کار نخواهند کرد. به طور کلی یک میانکنش شیمیایی و به طور اختصاصی هیدرولیز ATP ،یک چنین نیرویی را نمی تواند تولید کند، پس موتورهای ملکولی نمی توانند برپایه ی حرکت جهت دار برپایه القای مداوم انرژی حاصل از هیدرولیز ATP باشند.
ساختارهای سوم و چهارم پروتئین ها بیش تر به وسیله ی میانکنش های ضعیف شامل پیوندهای هیدروژنی، واندروالس، آبدوست و آب گریز تعیین می شوند. این ساختارها مستعد متحمل شدن اثرات بی نظمی های حرارتی هستند چون انرژی که مرتبط با این میانکنش ها است، بسیار کم هستند. بنابراین پروتئین ها، ملکول های پویایی هستند که به صورت مداوم نوسانات دمایی کنفورماسیون خود را نشان می دهند. این نوسانات دمایی در حول یک سری کنفورماسیون خاص با کم ترین انرژی آزاد رخ می دهند. انرژی شیمیایی ذخیره شده درون ملکول های ATP (و دیگر ملکول های از لحاظ انرژی شارژ شده)، مستقیما برای کار مکانیکی استفاده نمی شوند ولی در عوض مسئول مسیردهی حرکت دمایی ( Rectifying thermal motion ) یا انتشار آن در عناصر موتوری هستند.
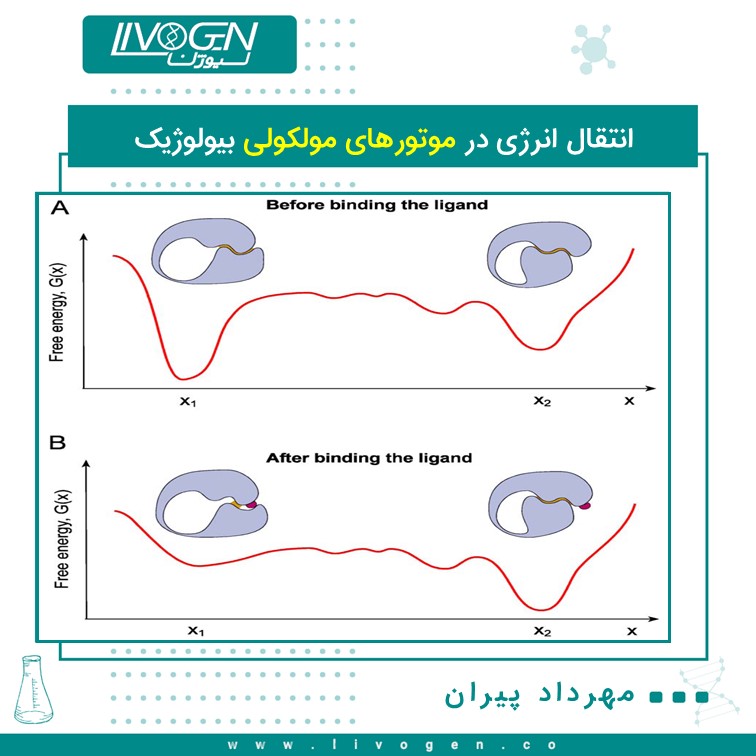
یک راه اثرگذاری روی انرژی آزاد، به وسیله ی اتصال یک لیگاند کوچک به یک سایت پروتئینی خاص مشخص می شود. در نتیجه ی اتصال، توزیع کنفورماسیونی به وسیله تغییر در پتانسیل انرژی آزاد تغییر می کند. بنابراین پروتئین متحمل یک تبدیل آلوستریکی ( Allosteric transition ) می شود. این بدین معنی است که معمولا اتصال در یک جایگاه پروتئین تغییر کنفورماسیونی را در یک جایگاه متفاوت دیگر القا می کند. یک تبدیل آلوستریکی نتیجه ی یک حرکت حرارتی بی نظم روی یک منظره¬ی (landscape) جدید انرژی آزاد است که به وسیله ی متصل شدن یا آزاد شدن لیگاند خلق می شود.
نویسنده :
| مهرداد پیران |